|
用於乙肝功能性治愈的BRII-835 + PEG-IFN-α聯合療法對照PEG-IFN-α的2期研究已完成首例患者首次給藥
將於2023年底前啟動多項研究中的首個研究,以探索BRII-179在具有顯著內在抗HBsAg反應患者中的治愈性療法潛力
PreHevbri®在亞太國家和地區的注冊申請及上市准備工作正在進行中
PreHevbri®帶來的近期收入機會以及充足的現金將支持公司至少運營至2026年
公司將於8月23日上午8:00(香港時間)/ 8月22日晚間8:00(美東時間)召開業績發布電話會議。慢乙肝藥物研發研討會(HBV R&D Day)將於8月24日下午1:00-2:30(香港時間)舉辦
中國北京和美國北卡羅萊納州達勒姆市2023年8月22日 /美通社/ — 騰盛博藥生物科技有限公司(「騰盛博藥」,「我們」或「公司」,股票代碼:2137.HK),一家致力於針對患者未被滿足的需求以及重大公共衛生性疾病開發創新療法的跨國企業,今日發布了公司最新進展和截至2023年6月30日止六個月的中期業績報告。
傳染性疾病治療領域
近期,騰盛博藥與VBI Vaccines Inc.(納斯達克股票代碼:VBIV)達成了兩項戰略協議,獲得了BRII-179的全球獨家許可,將具有臨床差異化的乙肝預防性疫苗PreHevbri®引入亞太國家和地區。
PreHevbri®的引入不僅充實了騰盛博藥已有的乙肝功能性治愈產品組合,也進一步推進了公司在大中華區及其他亞太國家和地區減少HBV傳播的解決方案。目前,公司正積極為 PreHevbri®在亞太市場上市做准備工作,其中優先考慮那些可能不需要額外試驗的國家和地區。目前,針對香港的市場注冊申請已經提交,預計監管機構將在近期做出決定。
今年6月,騰盛博藥的戰略合作伙伴Vir Biotechnology, Inc.(納斯達克股票代碼:VIR)在2023年歐洲肝髒研究協會(EASL)大會上分享了VIR-2218(BRII-835)和VIR-3434(BRII-877)的2期MARCH試驗A部分數據。數據顯示,慢性HBV患者的乙肝表面抗原(HBsAg)水平顯著下降,90%的患者HBsAg水平低於10 IU/mL,這表明VIR-3434(BRII-877)在慢性HBV治療中具有廣闊的潛力。隨著這些數據的公布,騰盛博藥於2023年8月獲得了中國國家藥品監督管理局(NMPA)藥品審評中心(CDE)對BRII-877(VIR-3434)1 期研究的新藥臨床試驗(IND)批准。
此外,在EASL大會上公布的令人信服的數據強調了BRII-835(VIR-2218)/PEG-IFN-α組合作為治療慢性HBV感染的同類最佳功能性治愈療法的潛力。值得注意的是,數據表明,治療結束時較高的抗HBs抗體應答與治療後24周持續的HBsAg清除有關,這表明患者的體液免疫在持續控制HBV感染方面的重要作用。
基於這一重要洞見,在獲得包括中國國家藥品監督管理局(NMPA)在內的多個亞太地區監管機構的批准後,騰盛博藥啟動了一項隨機、陽性對照的BRII-835 + PEG-IFN-α聯合療法的2期研究。該研究的主要目標是比較BRII-835/PEG-IFN-α聯合療法與單用PEG-IFN-α在功能性治愈率上的表現。公司還計劃將之前曾接受BRII-179治療並有抗HBsAg反應記錄的患者納入研究。公司相信,BRII-179具有獨特的能力,可以區分具有顯著自身體液免疫應答的患者和不具備這種能力的患者。此外,公司還在計劃開展更多研究,以探究BRII-179在激發更強抗體反應方面的作用,以及在廣泛的HBV患者群體中為BRII-835/PEG-IFN-α及其他聯合療法等治愈性療法拓展其適用患者的情況。
在另一項與Qpex的交易中,騰盛博藥獲得了BRII-693(此前也稱為QPX9003)的全球獨家權益,這是一種潛在的同類最佳合成脂肽靜脈注射抗生素,用於治療難治性多重耐藥(MDR)/廣泛耐藥(XDR)革蘭氏陰性菌感染(尤其是耐碳青霉烯類鮑曼不動桿菌和銅綠假單胞菌),從而鞏固了公司應對抗生素耐藥性挑戰的承諾,並進一步強化了財務支持。
中樞神經系統疾病治療領域
在與美國食品和藥物管理局(FDA)達成協議後,公司將於2023年第三季度啟動BRII-296用於治療產後抑郁症(PPD)的2期臨床試驗,以研究這種首創的長效、單次治療方案。BRII-296代表著患者治療模式的轉變,有望快速、持續地緩解新媽媽的抑郁症狀。據估計,僅在美國就有約50萬名母親患有PPD,全球有近2,000萬名女性受到PPD的困擾。
此外,公司還在繼續推進第二種長效注射劑BRII-297的首次人體1期臨床研究,擴大了各種焦慮和抑郁症或適應症的潛在突破性治療選擇。
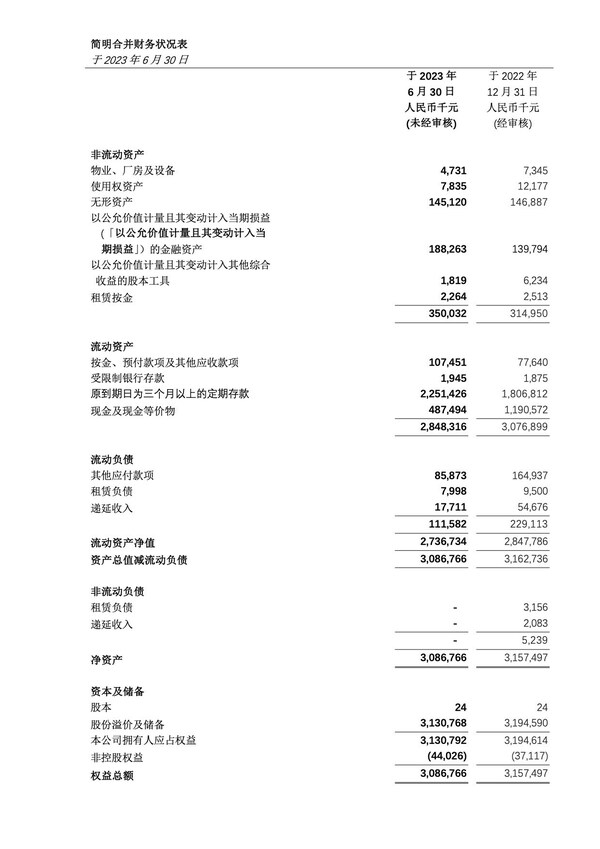
2023年中期財務業績
- 2023年上半年的其他收入為人民幣8,590萬元,與2022年上半年的人民幣 3,820萬元相比,增加了人民幣4,770萬元,增幅為124.9%。收入增加的主要原因是增加了原始期限超過三個月的定期存款,銀行利息收入增加了人民幣3,610 萬元,以及確認的中國政府補助收入增加了人民幣1,160萬元。
- 2023年上半年的研發支出為人民幣2.022億元,與2022年上半年的人民幣2.585億元相比,減少了人民幣5,630萬元,降幅為21.8%。減少的主要原因是由於公司決定終止COVID-19項目後,第三方承包費用的減少。
- 2023年上半年的行政支出為人民幣1.028億元,與2022年上半年的人民幣9,550萬元相比,增加了人民幣730萬元,增幅為7.6%。增加的主要原因是員工人數和電腦軟件費用的增加。
- 2023年上半年的綜合支出總額為人民幣1.04億元,與2022年上半年的人民幣2.177億元相比,減少了人民幣1.137億元,降幅為52.2%。減少的主要原因是其他收入增加,研發支出減少。
電話會議信息
公司將於香港時間2023年8月23日上午8:00(美國東部時間2023年8月22日晚間8:00)舉行電話會議。參會者須在電話會議之前完成注冊。注冊鏈接請點擊這裡。
關於騰盛博藥
騰盛博藥(股票代碼:2137.HK)是一家商業化階段的生物技術公司,致力於針對存在巨大未被滿足的患者需求、治療手段有限,以及給患者帶來嚴重社會歧視的重大公共衛生挑戰開發創新療法。公司專注於傳染性疾病和中樞神經系統疾病,正在推進一條涵蓋多種獨特候選藥物的產品管線,並通過領先的項目開發針對乙型肝炎病毒(HBV)感染的新型功能性治愈方案,和針對產後抑郁症(PPD)以及重度抑郁症(MDD)的首創治療方案。在富有遠見卓識和經驗豐富的領導團隊帶領下,公司在位於羅利-達勒姆、舊金山灣區、北京和上海的主要生物技術中心開展業務。欲了解更多信息,請訪問www.briibio.com。
前瞻性聲明
本新聞稿中傳達的信息包含某些具有或可能具有前瞻性的陳述。這些陳述通常包含諸如「將」、「期望」、「相信」、「計劃」和「預期」等詞語以及類似含義的詞語。就其性質而言,前瞻性陳述涉及風險和不確定性,因為它們與事件相關並取決於未來將發生的情況。可能存在目前被認為不重要或公司未意識到的其他重大風險。這些前瞻性陳述並非對未來業績的保證。在這些不確定性的背景下,讀者不應依賴這些前瞻性陳述。前瞻性陳述可能更新或根據未來的事件或發展進行相應修改,對此公司不承擔任何責任。
新聞來源:PR Newswire
以上新聞投稿內容由PR Newswire 美通社全權自負責任,若有涉及任何違反法令、違反本網站會員條款、有侵害第三人權益之虞,將一概由PR Newswire 美通社承擔法律及損害賠償之責任,與新頭條Thehubnews無關。